Одной из главных проблем медицины в последние годы стало отсутствие новых поколений антибиотиков. Эволюция бактерий постепенно делает их устойчивыми к антибиотикам. Такие микроорганизмы принято называть супербактериями. Ежегодно от них умирают десятки тысяч человек, так как эффективных методов лечения подобных инфекций не существует. С каждым годом ситуация усугубляется, так как количество видов супербактерий увеличивается. По некоторым оценкам специалистов, к 2050 году в мире от них будет умирать порядка 10 миллионов человек, если ничего не изменится в медицине. Решением этой проблемы могут стать антибиотики нового поколения, к которым у бактерий еще не выработалась устойчивость. И похоже, такие антибиотики от некоторых патогенов уже удалось найти.
Ученые получили антибиотик нового поколения, эффективный против супербактерий
Как супербактерии противостоят антибиотикам
Антибиотики обычно проникают сквозь клеточную мембрану, которая служит оболочкой инфекционных бактерий. Оказавшись внутрь клетки, они блокируют ее жизненно важные механизмы. Таким образом они вызывают либо гибель бактерий, либо не дают ей размножаться.
Однако некоторые бактерии имеют “защиту”, в результате чего антибиотик не может проникнуть сквозь мембрану. Например бактерия Acinetobacter baumannii (Crab), которая классифицируется Всемирной организацией здравоохранения как патоген “приоритета №1”, имеет двухслойную клеточную стенку. Чтобы проникнуть внутрь бактерии, антибиотикам необходимо преодолеть сразу два слоя, что очень сложно.
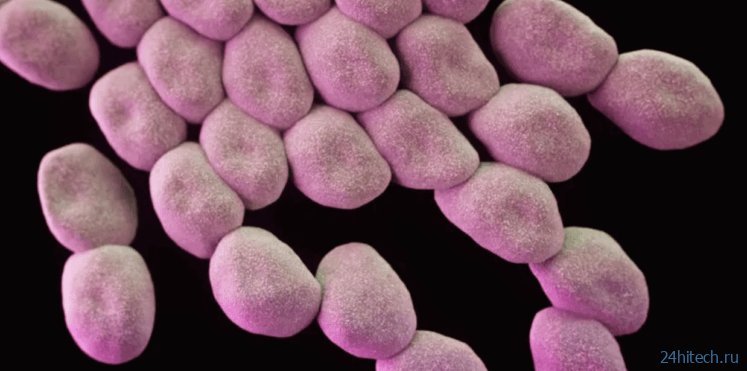
Бактерии Acinetobacter baumannii устойчивы к существующим антибиотикам
По оценкам ученых, краб убивает до 60% зараженных им людей. Эта бактерия обычно вызывает инфекцию мочевыводящих путей, дыхательных путей, а также кровотока, в результате чего часто приводит к сепсису. На Acinetobacter baumannii приходится 20% инфекций, которыми заражаются в больницах, домах престарелых, и прочих медицинских учреждениях.
Эффективными против этой бактерии всегда были антибиотики на основе пенициллина, мишенью которых является именно клеточная стенка. Эти антибиотики называются карбапенемами. Впервые их получили из пенициллина почти 50 лет назад. С тех пор они активно применяются в медицине, единственное, за это время подвергались химической модификации, которая повышала их эффективность по мере эволюции бактерий.
Но в конечном итоге супербактериальная версия Acinetobacter baumannii научилась расщеплять карбапенемы. В результате антибиотики стали совершенно неэффективны.
Новый антибиотик заставляет бактерию уничтожать саму себя
Новый класс антибиотиков
Зосурабальпин, новый класс антибиотиков, показал высокую эффективность в лабораторных условиях на колониях бактерий, а также во время испытаний на животных. Препарат способен убивать все штаммы Acinetobacter baumannii, в том числе уничтожает бактерии в кровотоке мышей, предотвращая развитие сепсиса.
Бактерия способна вырабатывать токсин, именуемый липополисахаридом, который служит инструментом для заражения. Он встраивается во внешнюю клеточную стенку. Зосурабальпин блокирует механизм, который отвечает за транспортировку токсина от внутреннего барьера бактерии к внешнему. В результате липополисахаридом начинает накапливаться внутри самой бактерии, в результате чего она гибнет. Как поясняют ученые, бактерия “вытаскивает чеку из собственной гранаты, которая ее убивает”. Об этом сообщает издание Scince Alert.
Но есть и плохая новость — антибиотик убивает только “крабовые” бактерии. На другие типы патогенов он не действует. Соответственно, медикам необходимо будет точно диагностировать тип инфекции, и только после этого применять новый антибиотик.
Новый антибиотик проходит первую стадию клинических испытаний
Но самое главное, новый препарат еще не протестирован на людях. Ученые только приступили к первой фазе клинических испытаний. Это значит, что еще неизвестны побочные эффекты и потенциальная токсичность препарата. Кроме того, неизвестно, насколько он эффективно борется с инфекцией в организме людей. Но даже, если препарат успешно пройдет испытания, прежде чем он попадет в продажу, пройдет довольно много времени.
Напоследок напомним, что недавно ученые обнаружили закономерности в эволюции ДНК видов. По мнению ученых, новое открытие поможет бороться с устойчивостью бактерий к антибиотикам. Поэтому, вполне возможно, что в ближайшем будущем проблема супербактерий будет решена полностью.




Нет комментарий