Мягкие «3D напечатанные» микромашины могут быть имплантированы в тело, чтобы регулярно поставлять нужные дозы лекарств.
Когда швейцарские часовщики изобрели «женевский двигатель» (двух шестерёночный механизм, который производит точное «тиканье»), они, наверное, никогда не предполагали, что биоинженеры однажды изготовят 15-миллиметровую версию «женевского двигателя» из мягкого гидрогеля. Но раньше и не пытались создать биологически совместимую микромашину, которая может быть имплантирована в тело, чтобы регулярно поставлять дозы лекарства «in vivo» (прямо в живом организме).
Этот странный биоробот создан в лаборатории Сэмюэля Сиа, преподавателя биоинженерии в Колумбийском университете в Нью-Йорке. Робот вживляется в тело и по команде поставляет дозу лекарства. При этом робот управляется снаружи и не использует ни проводов, ни аккумуляторной батареи. Это – устройство, которое хорошо удовлетворяют требованиям персонализированной медицины. Разработчик устройства говорит, что «Врачи хотят видеть, как пациент лечится, и затем, при необходимости, изменить тактику лечения». Робот уже был опробован на лабораторных мышах с раком костей и показал захватывающие результаты. Расскажем подробнее о роботе и результатах эксперимента. Разработчики сначала должны были изобрести тип «3D печати», чтобы можно было изготавливать произвести крошечные «женевские двигатели» и другие мягкие детали микромашин. Они придумали установку, которая наносит слои гидрогеля, в результате чего получаются эластичные твердые формы. Пока сборка микромашины производится вручную. Но, как говорят разработчики, этот процесс может быть автоматизирован. Но даже при ручной сборке, процесс печати и сборки микромашины занимает меньше, чем 30 минут. Сегодняшние типичные 3D принтеры потратили бы несколько часов, чтобы создать подобное устройство, потому, что они не могут обработать мягкие материалы, такие как гидрогель.
Устройство работает подобно механическим часам. Мягкий «женевский двигатель» регулярно производит «щелчки вперед», когда внешний магнит перемещает простой механизм, который является эластичной деталью со встроенными железными наночастицами (черная кривая часть на видео). С каждым щелчком, одна из шести камер выстраивается в линию с отверстием, через которое доза лекарства вытекает наружу. На видео, магнит (серебряный диск) приводит устройство в действие постоянно, чтобы продемонстрировать работу механизма. Но в клиническом использовании, врач может применить магнит только тогда, когда требуется очередная доза лекарства.
Можно задавать вопрос: может ли вживлённая в человеческий организм микромашина случайно приведена в действие внешним магнитом (или злонамеренно другим человеком с магнитом)? Такой риск существует, поэтому исследователи рассматривают другие способы приведения в действия механизма, в частности, ультразвук.
Самой сложной частью процесса проектирования была выбор подходящего биосовместимого материала. В отличие от твердых кремниевых или металлических устройств, очень гибкие и мягкие материалы совместимы с мягкими внутренностями тела. Но если такой материал разрушается как желе, трудно из него сделать робота. Материал должен быть достаточно жестким, чтобы работать как крошечная вживляемая микромашина.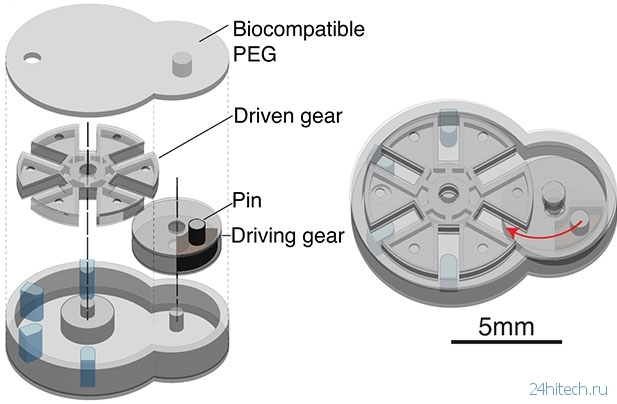
На рисунке показано устройство биоробота в разобранном (слева) и собранном (справа) состояниях. Верхняя и нижняя детали – корпус, под верхней крышкой корпуса видна ведомая шестерня (driven gear) с прорезями, рядом расположена ведущая шестерня (driving gear) со штифтом (pin). Максимальный габаритный размер устройства порядка 15-ти мм.
На рисунке ниже показано флуоресцентное изображение устройства, вживлённого (in vivo) в лабораторную мышь. 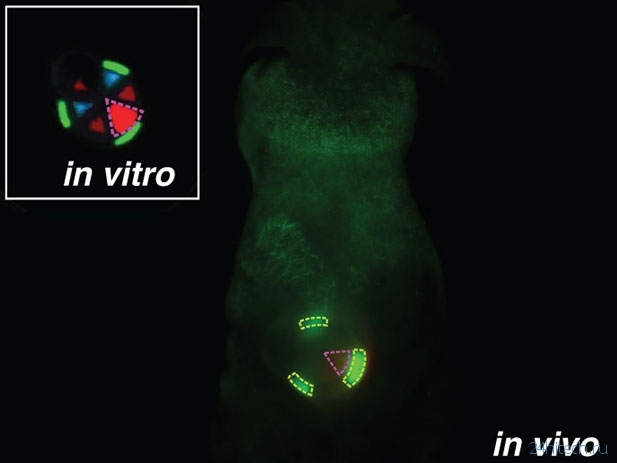
Клинические возможности устройства кажутся очевидными. Врачи-онкологи при помощи этого устройства могли бы с нужной периодичностью поставлять в организм более концентрированные дозы сильных противораковых лекарств или гормонов (например, при недостаточности щитовидной железы или сахарном диабете).



Нет комментарий